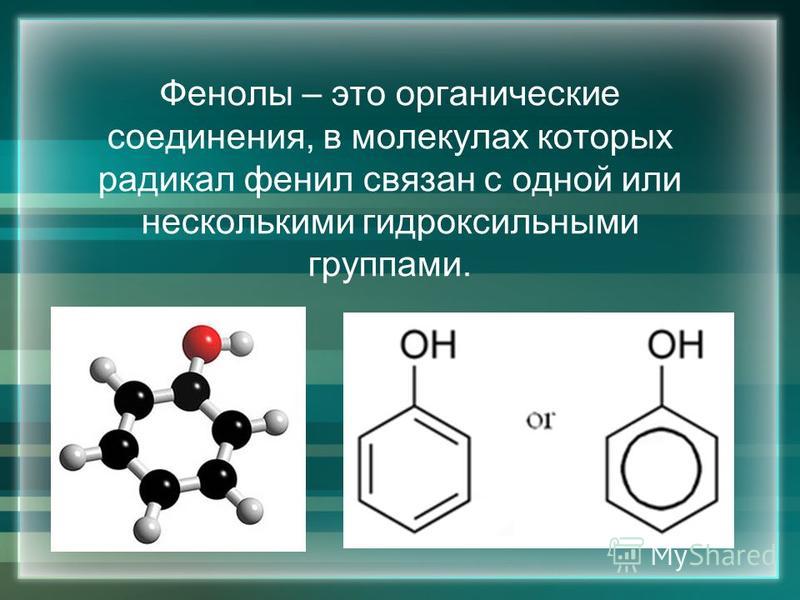
План урока Фенолы Классификация фенолов Строение молекулы Физические свойства фенола Химические свойства. Скачать бесплатно и без регистрации. Одноатомные фенолы содержат в молекуле одну гидроксильную группу (фенол) Двухатомные фенолы содержат две гидроксильные группы (1,3- дигидроксибензол, мета- дигидроксибензол, резорцин) Трёхатомные фенолы содержат три гидроксильные группы Классификация фенолов. По количеству бензольных колец фенолы бывают моноядерные и многоядерные На план урока.
Номенклатура При составлении названия фенолов нумерация атомов углерода в бензольном ядре начинается с атома непосредственно связанного с гидроксильной группой. Затем называются заместители, начиная с простейшего, с указанием номера атома углерода, при котором они находятся. Вследствие частичного окисления на воздухе он бывает окрашен в розовый цвет. Его температура плавления +4. Фенол обладает резким характерным запахом.
В холодной воде он мало растворим, но уже при 7. Фенол ядовит! При попадании на кожу вызывает ожоги поэтому с фенолом необходимо обращаться осторожно! Диссоциация фенола Влияние бензольного кольца на гидроксильную группу выражается в том, что связь атома водорода с кислородом ослабевает, и фенол способен диссоциировать в водном растворе. Взаимодействие с натрием Фенол, как и спирты, взаимодействует с металлическим натрием с образованием соли (фенолята натрия) и водорода. Взаимодействие со щелочами Влияние бензольного ядра обуславливает свойство, которое совсем на характерно для спиртов, фенол может взаимодействовать со щелочами, проявляя свойства слабой кислоты.

Качественная реакция на фенол – взаимодействие с хлоридом железа (III); 10. Презентация к уроку "Источники права" 10 класс, Боголюбов. Фенол". Презентация к уроку химии 10 (базовый) по теме .
Презентация к уроку "Политическое поведение" 11 класс. Фенол". Презентация к уроку химии 10 (базовый) по теме .
Скачать бесплатные презентации по химии для 10 класса Вы можете на. Презентация на тему «Строение органических соединений» является. Скачать презентацию Фенолы Презентация написана на тему: «ФЕНОЛЫ». Органическая химия. Спирты, алканолы. Ароматический спирт - фенол - Duration: 2:32.
Фенол – кислота довольно слабая, более сильные кислоты вытесняют фенол из фенолятов. Реакции окисления Фенол окисляется кислородом воздуха, приобретая фиолетовую окраску. Реакции замещения. Голомидова Марина Учебник Японского Языка Для Детей. Галогенирование – для фенола характерны реакции замещения с галогенами. Они проходят значительно легче, чем реакции замещения бензола.
4 Фенолы классифицируют по атомности, т.е. Одноатомные фенолы содержат в молекуле одну гидроксильную . Презентация к уроку химии 10 (базовый) по теме "Каменный уголь.Фенол" Дается. Фенол". Презентация на тему "Феноли" до уроку з х. Проект на тему: “Феноли” 11 . Презентация на тему: Фенол. Скачать эту презентацию. Фенол проявляет свойства слабой кислоты : Взаимодействует с щелочными металлами и . Описание слайда: Классификация фенолов Фенолы классифицируют по атомности, т.е. Одноатомные фенолы .

При этом почти всегда образуются тризамещённые производные – в положениях 2,4,6. Нитрование фенола Нитрование фенола также происходит легче, чем нитрование бензола. В зависимости от концентрации азотной кислоты условия реакции и получаемые продукты могут быть разными.
В XIX столетии её применяли в качестве жёлтого красителя до случая, когда в Париже (1. В результате чего образуется предельный циклический спирт – циклогексанол. Реакции гидрирования.
Реакции поликонденсации с альдегидами На план урока. Качественная реакция на фенол. Формулы. На план урока. Получение фенола 1. Фенол выделяют из каменноугольной смолы.
Однако потребность в феноле настолько велика, что этого источника оказывается недостаточно. Синтез фенола из бензола На план урока.
Применение фенола. Фенол применяют для производства фенолформальдегидных пластмасс, синтетического волокна капролактам, красителей, лекарств, взрывчатых веществ и других продуктов. Раствор фенола в воде обладает дезинфицирующими свойствами На план урока. Чем опасен фенол. Практически сразу после получения фенола ученые установили, что это химическое вещество обладает не только полезными свойствами, что позволяет его использовать в различных сферах науки и производства, но и является сильнодействующим ядом. Так, вдыхание паров фенола в течение непродолжительного времени может привести к раздражению носоглотки, ожогам дыхательных путей и последующему отеку легких с летальным исходом.
При соприкосновении раствора фенола с кожей образуются химические ожоги, которые впоследствии трансформируются в язвы. Эти дома в свое время считались экспериментальными.
В бетон, использованный при их строительстве, добавляли фенолформальдегид. Это должно было ускорить его затвердевание и тем самым приблизить сроки сдачи домов. Новоселы, поначалу обрадовавшиеся просторным квартирам, вскоре поняли, что вместе с новым жильем они получили целый букет проблем со здоровьем – это и аллергия, и болезни глаз, почек, дыхательных путей, и даже злокачественные новообразования. Дело в том, что фенол и его производные без труда проникают в организм человека через кожу и желудочно- кишечный тракт, а пары фенола – через легкие. В организме фенол легко образует соединения с другими веществами, присутствующими в организме. Чем выше концентрация фенола в крови, тем сильнее его неблагоприятное влияние на здоровье человека. Хроническое отравление фенолом угрожает не только жителям «фенольных домов».
Недобросовестные изготовители мебели, строительных и отделочных материалов, лакокрасочных изделий, декоративной косметики. Помните, если вас настораживает неприятный запах недавно приобретенной вещи, если вам кажется, что ваше здоровье после покупки мебели или недавнего ремонта пошатнулось, будет лучше вызвать специалиста- эколога, который проведет все нужные исследования и даст необходимые рекомендации. Хроническое отравление фенолом вызывает поражения центральной нервной системы, нервные расстройства, сопровождаемые головными болями и потерей сознания, а также поражения почек, печени, органов дыхания и сердечно- сосудистой системы.